9. Sınıf Kimya konuları ve müfredatı

Yayınlanma:
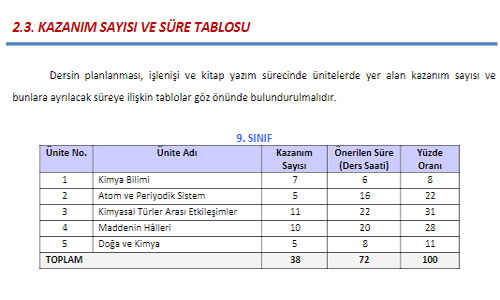
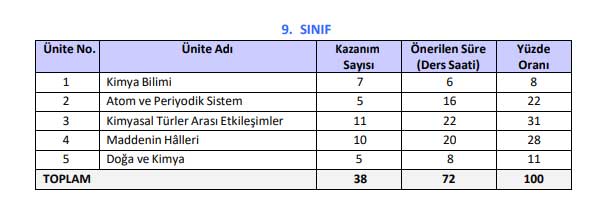
9. Sınıf Kimya konuları ve müfredatında neler var, 1. Ünite Kimya Bilimi, 2. Ünite Atom ve Periyodik Tablo, 3. Ünite Kimyasal Türler Arası Etkileşim, 4. Ünite Maddenin Halleri ve 5. Ünite Doğa ve Kimya, 38 Kazanım 72 saat.
9. Sınıf 1. Dönem Kimya Konuları
- Simyadan Kimya
- Kimya Disiplinleri
- Kimyacıların Çalışmaları
- Kimyanın Sembolik Dili
- Kimya Uygulamalarında İş Sağlığı ve Güvenliği
- Atom Modelleri
- Atomun Yapısı
- Periyodik Sitem
- Kimyasal Tür
- Güçlü Etkileşimler
9. Sınıf 2. Dönem Kimya Konuları
- Zayıf Etkileşimler
- Fiziksel ve Kimyasal Değişimler
- Maddenin Fiziksel Halleri
- Katılar
- Sıvılar
- Gazlar
- Plazma
- Su ve Hayat
- Çevre Kimyası
9. SINIF KİMYA ÜNİTE, KONU, KAZANIM VE AÇIKLAMALARI
9.1. KİMYA BİLİMİ
simya, kimya, madde, element, bileşik, sembol, formül, laboratuvarda güvenlik
9.1.1.Simyadan Kimyaya
9.1.1.1. Kimyanın bilim olma sürecini açıklar.
9.1.2. Kimya Disiplinleri ve KimyacılarınÇalışma Alanları
9.1.3. Kimyanın Sembolik Dili
9.1.4. Kimya Uygulamalarında İş Sağlığı ve Güvenliği
9.2. ATOM VE PERİYODİK SİSTEM
9.2.1. Atom Modelleri
9.2.2. Atomun Yapısı
9.2.3. Periyodik Sistem
9.3. KİMYASAL TÜRLER ARASI ETKİLEŞİMLER
9.3.1. Kimyasal Tür
9.3.1.1. Kimyasal türleri açıklar. Radikal kavramına girilmez.
9.3.2. Kimyasal Türler Arası Etkileşimlerin Sınıflandırılması
9.3.3. Güçlü Etkileşimler
9.3.4. Zayıf Etkileşimler
9.3.5. Fiziksel ve Kimyasal Değişimler
9.4. MADDENİN HÂLLERİ
9.4.1. Maddenin Fiziksel Hâlleri
9.4.2. Katılar
9.4.3. Sıvılar
9.4.4. Gazlar
9.4.5. Plazma
9.5. DOĞA VE KİMYA
9.5.1. Su ve Hayat
9.5.2. Çevre Kimyası
Müfredatın detaylarına buradan ulaşabilirsiniz. Tıklayınız
ÖDEV & BİLGİ DÜNYASI







Yorumların her türlü cezai ve hukuki sorumluluğu yazan kişiye aittir. Eğitim Sistem yapılan yorumlardan sorumlu değildir.